محاسبه pH در شیمی بسیار ضروری است و این اندازه گیری کاربردهای بسیار زیادی در علوم مختلف دارد. pH، اندازه گیری اسیدی یا بازی بودن یک ماده است. در زندگی روزمره ما با مایعات زیادی با pH متفاوت مواجه می شویم. آب یک ماده خنثی است و نوشابه اغلب اسیدی است. pH یک ویژگی مهم در زندگی و علوم مختلف است، زیرا بر نحوه تعامل مواد با یکدیگر و با بدن ما تأثیر می گذارد. در دریاچه ها و اقیانوس ها، pH تعیین می کند که چه موجوداتی قادر به ادامه حیات در آب هستند.
ایده pH در سال 1909 توسط یک شیمیدان دانمارکی به نام سورن سورنسن برای حل مشکل آزار دهنده ای که شیمیدانان با آن مواجه بودند، ارائه شد. شیمیدان ها دریافته بودند که وقتی با اسیدها و غلظت یون های هیدرونیوم کار می کردند، اعداد در محاسبات شامل نماهای منفی می شدند. سورنسون استفاده از لگاریتم منفی [+H3O] را برای اندازه گیری اسیدیته پیشنهاد کرد.
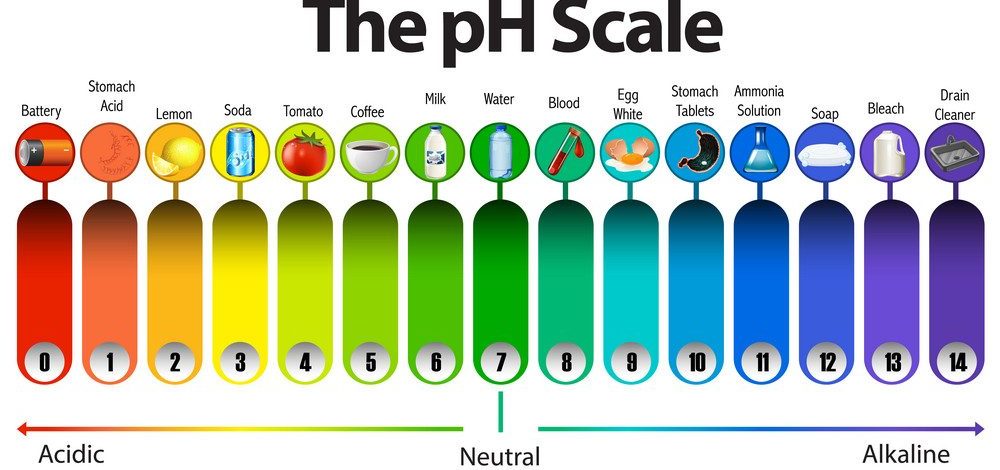
سورنسون اندازه گیری جدید را pH نامید. p مخفف قدرت و H برای هیدروژن است؛ بنابراین pH مخفف قدرت هیدروژن است. pH فقط مقداری است که برای بیان اسیدی یا بازی بودن یک محلول استفاده می شود. محاسبه pH در شیمی از 0 (کمترین مقدار ممکن) تا 14 (بالاترین مقدار ممکن) است. در نتیجه مقادیر 0-6 نشان دهنده اسیدی بودن، مقدار 7 نشان دهنده خنثی بودن و مقادیر 8-14 نشان دهنده بازی بودن هستند.
فهرست
pH چیست
محاسبه pH در شیمی اندازه گیری غلظت یون هیدروژن در یک محلول است. در نظریه برونستد لوری درباره اسیدها و بازها، ما اسید را به عنوان دهنده پروتون یعنی فقط یون هیدروژن بیان می کنیم. هرچه یک اسید قوی تر باشد، در اهدای پروتون بهتر عمل می کند، در نتیجه pH آن محلول کمتر می شود. با استفاده از مقیاس بالا، می توانیم بفهمیم که سرکه بالزامیک اسید بسیار قوی تری از صابون است.
هر چه غلظت یون هیدروژن در یک محلول بیشتر باشد، pH آن کمتر است و بالعکس. PH کمتر از 7 اسیدی و بیشتر از 7 قلیایی است. ممکن است در گذشته به شما گفته شده باشد که pH 7 خنثی است، اما در واقعیت، pH خنثی تعریف متفاوتی دارد. ماده اسیدی یک پروتون از دست می دهد و یک قلیایی یک پروتون را دریافت می کند. فرمول اندازه گیری pH عبارت است از:
pH = -log (H +)
مقیاس pH چیست
مقیاس pH از عدد 0 شروع می شود و به عدد 14 ختم می شود. اسیدی ترین مواد نزدیک به 0 خواهد بود، در حالی که قلیایی ترین مواد نزدیک به 14 خواهد بود. قلیایی ترین مواد دارای طبقه بندی بین 7 تا 14 خواهند بود. فرمول محاسبه pH در بالا نشان داده شده است و به عنوان پایه لگاریتم منفی 10 غلظت هیدرونیوم تعریف می شود.
از آنجایی که pH در یک مقیاس log است به این معنی که افزایش pH 1 برابر با ضرب غلظت یون +H در 10 است. بنابراین حتی اگر تفاوت بین pH 6 و pH 7 ممکن است کوچک به نظر برسد، اما در واقع بسیار قابل توجه است. برای معادله pH، غلظت یون هیدروژن همیشه یک غلظت مولی، یعنی مول +H در لیتر است.
نحوه محاسبه PH
اگر غلظت یون های هیدروژن را می دانید، برای محاسبه pH فقط کافی است آن را در معادله قرار دهید. گاهی اوقات، یک اسید به طور کامل به یون در محلول تجزیه می شود. به عنوان مثال، فرض کنید یک محلول مولی 0.2 اسید کلریدریک به طور کامل در یک محلول تجزیه می شود. این بدان معناست که برای هر مول اسید کلریدریک، 1 مول یون +H وجود دارد.
اسید کلریدریک یک اسید قوی است؛ بنابراین در محلول کاملا تجزیه می شود. در نتیجه غلظت یون های هیدروژن در محلول 0.2 مولار است. فرمول pH به ما می گوید که pH لوگاریتم منفی غلظت یون هیدروژن است. سپس از یک ماشین حساب برای محاسبه کردن 0.2 مولار به فرمول pH استفاده می کنیم.
pH = -log (H +) = – log (0.2) = 0.699
حال اگر اسید کاملا در محلول تفکیک نشد، باید ثابت تفکیک یا ثابت یونیزاسیون (ka) را که به شما داده می شود، در فرمول زیر برای تعیین مقدار pH قرار دهید.
pKa = -log(Ka)
pKa =10-pKa
ثابت یونیزاسیون نشان می دهد یک اسید چقدر ضعیف یا قوی است. هرچه مقدار این ثابت کمتر باشد، اسید قوی تر و توانایی آن برای اهدای پروتون هایش بیشتر می شود. یک اسید قوی ثابت تفکیک کمتر از صفر خواهد داشت. به طور دقیق تر pKa- پایه log منفی ده مقدار Ka است که از معادله بالا به دست می آید.