اتمها اساس عناصر هستند. تمام عناصر جدول تناوبی از اتم های مختلف ساخته شده اند و ساختار این اتمها طیفی از پدیده ها از واپاشی رادیواکتیو تا انرژی هسته ای را به همراه دارد. اتمها کوچک هستند. قطر یک اتم معمولی ده میلیاردم متر است. هسته یک اتم فقط یک چهار میلیاردم متر است.
تصویر اصلی یک هسته حاوی پروتون و نوترون است که توسط الکترون هایی احاطه شده است که به دور هسته می چرخند. این توصیف تقریباً درست است – به دلیل اصل عدم قطعیت در فیزیک کوانتومی، ما نمی توانیم در واقع مداری را برای یک الکترون تعریف کنیم، و در عوض آنها در یک ابر نامشخص به دور هسته ازدحام می کنند.
هر چه تعداد پروتون ها و نوترون های موجود در هسته اتم بیشتر باشد، آن عنصر سنگین تر است. بنابراین، برای مثال، سرب دارای 82 پروتون و بین 120 تا 132 نوترون در هسته خود است، در حالی که هیدروژن، سبک ترین عنصر، فقط یک پروتون و گاهی اوقات یک یا دو نوترون دارد.
تعداد پروتون ها در اتم هر عنصر معین همیشه یکسان است. فیزیکدانان به این عدد اتمی می گویند. تعداد نوترون های هسته می تواند تغییر کند و ما اتم های یک عنصر با تعداد نوترون های متفاوت را «ایزوتوپ» مینامیم. گاهی اوقات این ایزوتوپ ها پایدار هستند، اما اغلب ناپایدار هستند و در نهایت تجزیه می شوند.
فهرست
تاریخچه کشف اتم
از اوایل دهه 1800 عناصر به واحدهای بنیادی با وزن معین، در تئوری که توسط دانشمند انگلیسی جان دالتون مطرح شد تجزیه می شوند. او این واحدها را ذرات بنیادی و غیرقابل تقسیم می دانست، به همین دلیل از کلمه یونانی «اتوموس» استفاده کرد.
همه چیز در سال 1897 جالب تر شد، زمانی که تامسون الکترون ها را کشف کرد، با فهمیدن اینکه پرتوهای کاتدی جریان هایی از ذرات هستند و نه امواج الکترومغناطیسی. این کشف از اهمیت فوق العاده ای برخوردار بود زیرا به این معنی بود که اتمها ذرات بنیادی نیستند و می توانند از ذرات کوچکتر تشکیل شوند.
با این حال، اتمها از نظر الکتریکی خنثی هستند، در حالی که الکترون ها دارای بار منفی هستند. بنابراین تامسون، منطقی فکر کرد که باید چیزی درون اتم با بار مثبت وجود داشته باشد که بارهای منفی الکترون ها را خنثی می کند. آنچه او در نظر داشت «مدل پودینگ آلو» نام داشت که الکترون هایی مانند آلو در پودینگی بار مثبت جاسازی شده بودند.
ساختار اتمی چیست؟
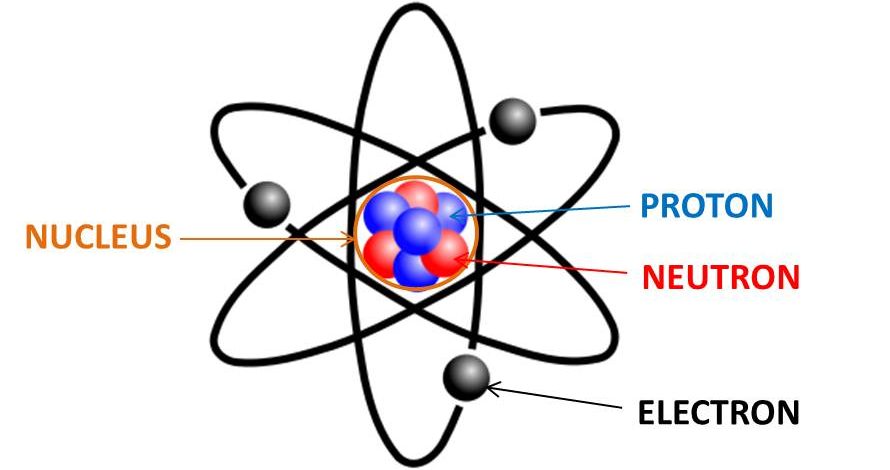
ساختار اتمی ساختار یک اتم است – یعنی یک هسته با بار مثبت که الکترون هایی با بار منفی دور آن می چرخند. اتمها از سه ذره ساخته شده اند:
- پروتون ها
- نوترون ها
- الکترون ها
پروتون ها و نوترون ها هسته را تشکیل می دهند. در حالی که الکترون ها دور هسته می چرخند. تعداد پروتون ها و الکترون های یک اتم نوع عنصر را مشخص می کند. به عنوان مثال، هیدروژن از یک پروتون با بار مثبت و یک الکترون با بار منفی تشکیل شده است که دور هسته می چرخد.
در جدول تناوبی عدد اتمی بالای هر عنصر به ما می گوید که چند پروتون در هسته وجود دارد. از آنجایی که اتم ها دارای تعداد الکترون های برابر با پروتون ها هستند، عدد اتمی نیز می تواند به ما بگوید که یک اتم چند الکترون دارد.
جرم اتمی عددی است که در پایین هر عنصر قرار دارد. با کم کردن عدد اتمی از جرم اتمی، تعداد نوترون هایی که در هسته یافت می شوند به دست می آیند.
چگونه اتم ها یونیزه می شوند
الکترون ها همیشه به پوسته های خاص خود محدود نمی شوند. اگر یک اتم فوتون نور را با انرژی کافی جذب کند – مثلاً یک فوتون فرابنفش – این انرژی جذب شده می تواند باعث شود یک الکترون برای مدت کوتاهی به سطح انرژی بالاتر منتقل شود. با این حال، این یک وضعیت ناپایدار است، بنابراین الکترون به پایین میافتد و در حین انجام این کار، انرژی جذب شده را در طول موج مشخصه آن اتم آزاد میکند.
گاهی اوقات، انرژی جذب شده توسط اتم هنگام برخورد یک فوتون، نه تنها باعث می شود که یک الکترون به سطح انرژی بپرد، بلکه به الکترون اجازه دهد تا از اتم جدا شود. نتیجه خالص این است که اتم خنثی قبلی بار الکتریکی پیدا میکند، زیرا تعداد پروتونها اکنون یک عدد از تعداد الکترونها بیشتر میشود (گاهی اوقات دو، اگر دو الکترون از بین بروند). این فرآیند یونیزاسیون نامیده می شود و اتم یونیزه شده یون نامیده می شود. به واسطه این فرآیند شما درخشش سحابی ها را در آسمان مشاهده می کنید.